肠道微生态之战:Crestone凭何破解艰难梭菌感染百年难题?
从1928年弗莱明首次发现青霉素,到四环素成为全球首个获批上市的广谱抗生素,再到科研人员在青霉素结构上引入氨基,进一步拓宽抗菌谱,人类在抗菌药物领域的探索已走过近百年。
其中,“广谱性”自始至终均是贯穿抗菌新药研发历程的核心追求,也是推动现代抗感染治疗进步的关键主线。
然而,曾被誉为现代医学里程碑的广谱抗生素,同时却也是一把双刃剑。其在挽救无数生命的同时,随着而来的也是被忽视的滞后性风险,且已成为抗菌治疗的重大挑战。
据最新CDI诊疗指南显示,由滥用广谱抗生素所导致的“艰难梭菌感染”便是最典型、最严峻的后果之一。
一场属于肠道微生态之战
在广谱抗生素的不良反应中,耐药(诱导超级细菌出现)与破坏肠道微生态平衡两者的后果最为突出,前者危害最烈,后者则较为常见。
而当前抗菌新药研发的主要方向,正是围绕这两大痛点所展开。
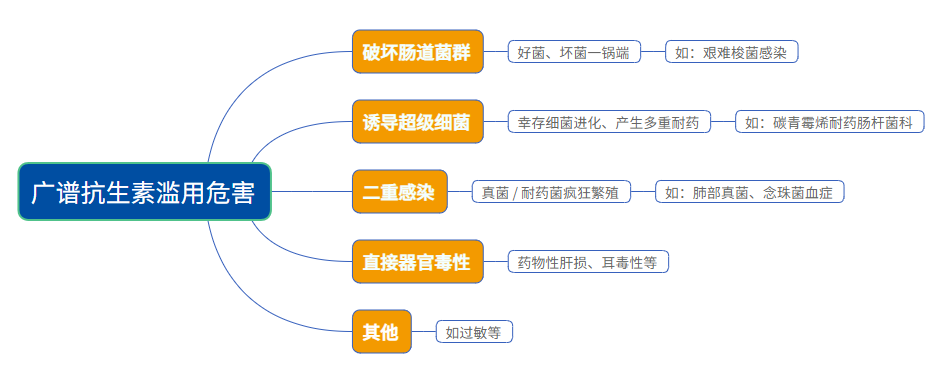
图:广谱抗生素滥用后果
数据来源:公开数据整理
据《Nature Reviews Microbiology》2025年发表的艰难梭菌感染(CDI)机制与防控综述内容显示,抗生素暴露作为艰难梭菌感染最主要的危险因素,其在清除致病菌的同时,会不可逆地破坏肠道微生态平衡,为艰难梭菌的入侵、定植、复发与再感染打开“方便之门”。
几乎所有抗生素的使用均会升高CDI发病风险,每年导致美国约223,900例CDI感染病例患者住院治疗,至少12,800人因此丧生。而讽刺的是,现有CDI一线治疗仍多以广谱抗生素为主,这也导致艰难梭菌的复发率长期以来居高不下(超20%)。
因此,临床界亟须既能精准清除病原体,又能最大限度保护肠道有益菌的新型疗法,大幅降低CDI感染的临床复发率。
Crestone:向艰难梭菌感染宣战
2009年,Crestone Pharma成立于美国科罗拉多州博尔德市,其创立之初就聚焦于开发针对严重细菌感染的新药,对临床需求性抗菌与抗生素耐药性的问题解决尤为在行。但其实,Crestone现有研发团队、技术平台与在研管线实际诞生时间却还要更早于企业成立。
人员方面,包括Crestone现任CEO、COO在内的多名联合创始人与企业高管均有着Replidyne的任职经历。
管线方面,两家公司均聚焦耐药菌感染、艰难梭菌、MRSA、结核等领域的全新作用机制小分子抗菌药,Crestone的管线很多程度上可以看做Replidyne管线的直接延续。


图:Crestone部分高管(具备Replidyne背景)
图片来源:Crestone官网
当然,青出于蓝而胜于蓝的是,Crestone通过数年基础研究和技术创新,逐步也建立起不同于Replidyne的独特药物研发平台,其研究成果在2024年先后亮相于第9届AMR Conference(瑞士巴塞尔)和ICDS 2024(斯洛文尼亚布莱德),并成功发表于《柳叶刀·传染病》 2026,展示了其在抗微生物耐药性领域的创新能力和技术实力。
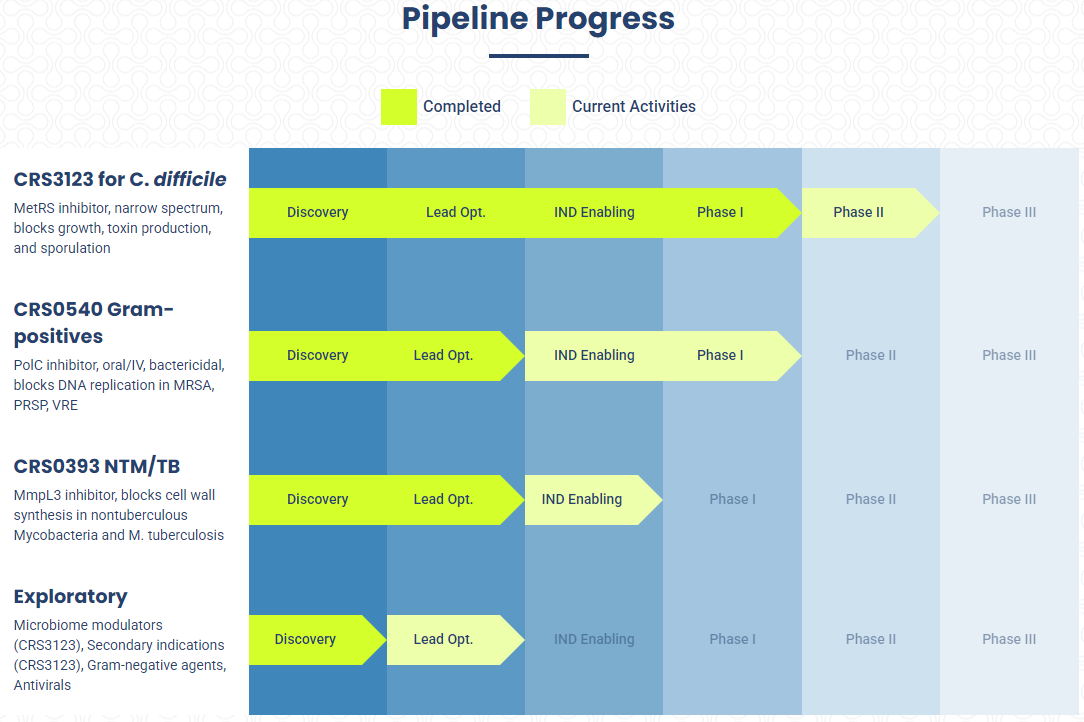
图片来源:Crestone官网
目前,Crestone已有三款核心管线进入了IND阶段,分别是针对艰难梭菌感染的CRS3123,现处于临床Ⅱ期阶段,并已准备好进入临床III期;针对耐药革兰氏阳性菌感染(如耐甲氧西林金黄色葡萄球菌、万古霉素耐药肠球菌等)的CRS0540,现处于临床I期阶段;针对非结核性分枝杆菌的CRS0393,目前处于IND阶段。
其中,CRS3123作为Crestone进展最快的管线,是现阶段企业最核心的资产,也是背负企业命运的关键,其重要性不言而喻。
CRS3132:对标万古霉素,优势显著
对于CRS3123而言,其乃是一种小分子蛋白质合成抑制剂,作用靶点为甲硫氨酰-tRNA合成酶(MetRS),该靶点仅存在于艰难梭菌等少数厌氧菌及部分革兰氏阳性需氧菌中,而对人体至关重要的拟杆菌、双歧杆菌等共生有益菌却并不表达,因此,理论上该疗法可实现“精准击敌、不伤友菌”。
在现有CDI临床治疗层面,2021年美国感染病学会(IDSA)联合美国医疗保健流行病学学会(SHEA)更新发布的成人CDI的管理指南中指出,对于初治患者而言,非达霉素为优选疗法、万古霉素为替代选择(受价格和药物可及性影响);对于初次复发患者,非达霉素仍为首选,万古霉素脉冲疗法为替代选择,Bezlotoxumab为辅助治疗选择;对于多次复发患者,则可在上述疗法之外,额外尝试“粪菌移植治疗”。
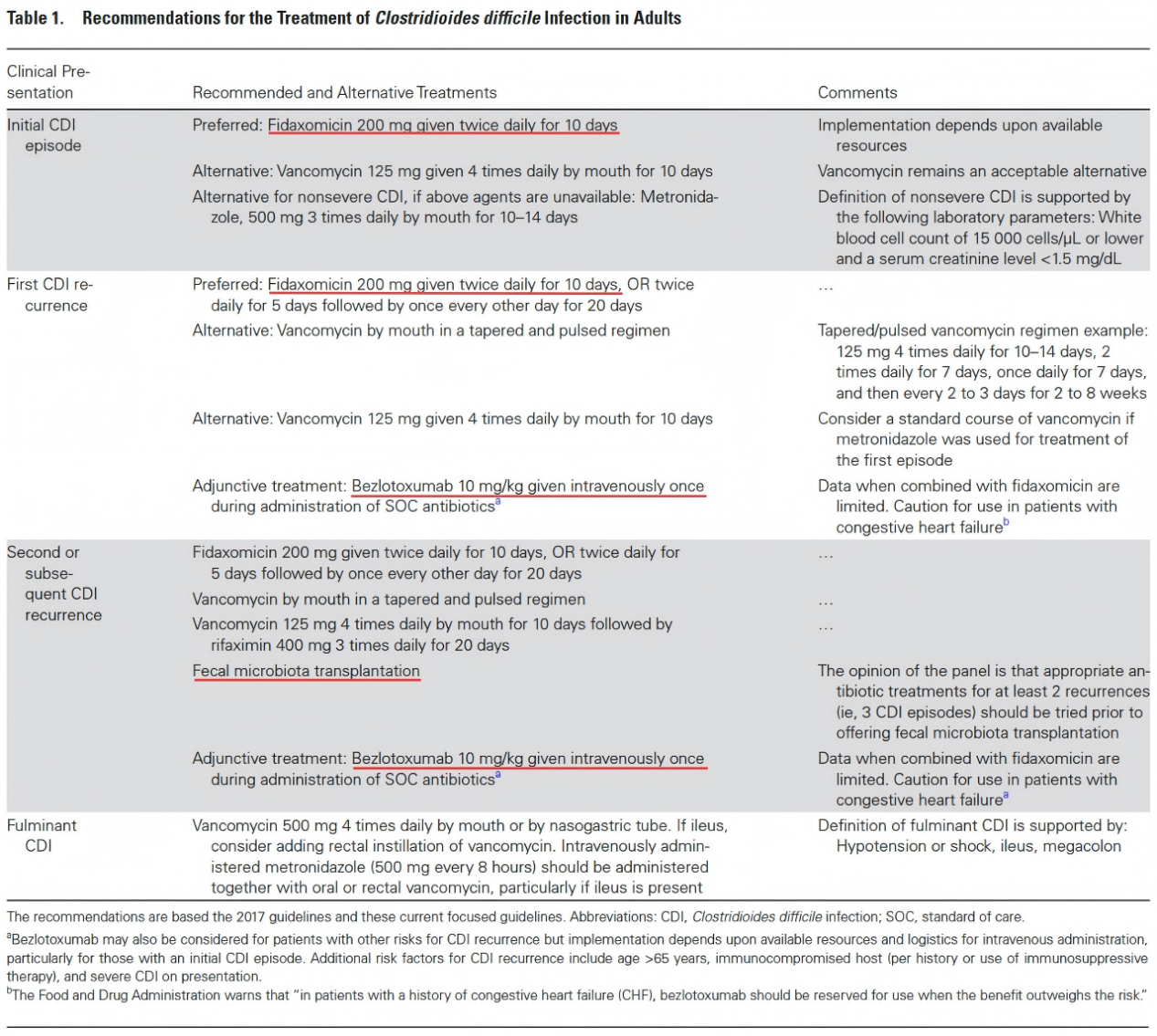
图片来源:IDSA/SHEA:成人艰难梭菌感染的管理指南2021[3]
该版指南与2017版的最大区别在于,不考虑药物治疗价格与可及性方面的情况下,聚焦了非达霉素(窄谱抗生素)和Bezlotoxumab(TCD单抗)在CDI治疗中的应用,并指出了粪菌移植疗法对CDI的正向作用,适当降低了万古霉素这类广谱抗生素在CDI治疗上的临床地位。
回顾CDI的临床治疗历程,其自1978年明确病因至今,领域先后经历了基础抗生素时代、精准药物时代、菌群修复时代、综合治疗时代四大阶段,治疗策略从单一抗菌逐步转向“抗菌+菌群重建+免疫调节”的综合模式。
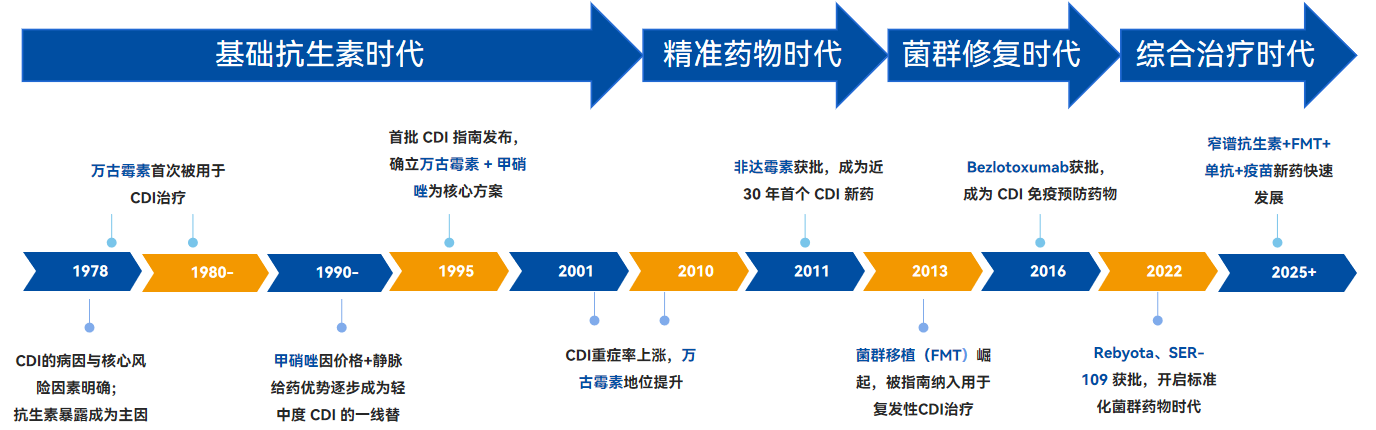
数据来源:公开数据整理
其中,现阶段获批的TCD单抗多被定位于“辅助治疗”,粪菌移植则多应用于临床后线的复发与二次复发治疗,至于临床一线的初治患者,其治疗方案仍多以“万古霉素与非达霉素”为主。
因此,理论上CRS3123的实际对标竞品应只有万古霉素与非达霉素两者,而以目前CRS3123所披露的临床数据来看,其与当下主流CDI疗法(目前是万古霉素)相比,具有诸多显著优势:
强杀菌:对所有临床分离出的艰难梭菌菌株都具有极强的杀灭效果。
抗菌谱较窄:与现有的治疗方法相比,有望显著减少对正常肠道菌群的破坏。
抑毒:可显著抑制毒素的产生,有望降低发病率和死亡率,并加快症状的缓解速度。
抑孢:可显著抑制孢子形成,有可能降低病毒的传播率和复发率。
差异性机制:由于疗法特殊的作用机制,导致其用药过程中对全身性抗生素(比如万古霉素)的疗效无影响。
在CRS3123一项耗时3年的多中心、双盲对照临床Ⅱ期实验中,43名患有初次或首次复发CDI的成年患者被随机分为三组,分别接受CRS3123(200mg或400mg,每日两次)或标准药物万古霉素(125mg,每日四次)治疗10天,结果显示CRS3123在有效性上展现出媲美万古霉素的临床治愈率以及更低的临床复发率。
有效性方面,经治12-15天后,CRS3123展现了不逊于万古霉素的实力,期间可迅速降低毒素及孢子计数(下图),在意向治疗人群中,200mg组和万古霉素组的治愈率均为93%,而400mg组则达到了100%。
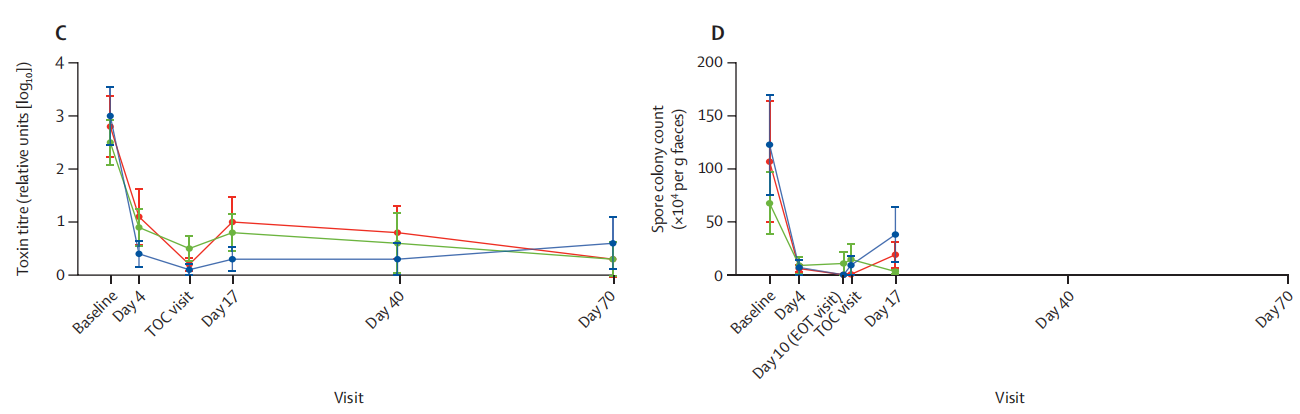
图C:经 CCNA 检测的艰难梭菌毒素A和B抗体平均滴度
图D:通过乙醇冲击法杀灭艰难梭菌细胞后培养评估的活孢子菌落计数
图片来源:Crestone官方资料[5]
复发率方面,在后续为期40天的随访过程中,CRS3123组的复发率呈现出更低的趋势,而这种复发率差异的情况,与研究团队预设的药物特性完全吻合。也充分证明了疗法作为窄谱抗生素,在强力抑制艰难梭菌的同时,对肠道中保护性的菌群干扰更小。
200mg组13名患者中无人复发(复发率0%)。
400mg组14名患者中1人复发(7%)。
万古霉素组13名患者中则有3人复发(复发率23%)。
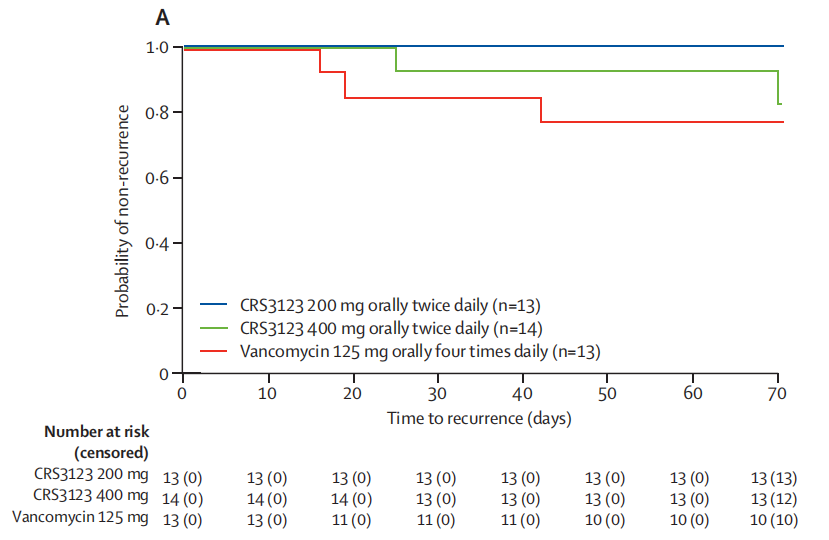
图A:复发情况的Kaplan-Meier曲线
图片来源:Crestone官方资料[5]
安全性方面,两组剂量组下,绝大多数治疗相关不良事件均为轻度至中度,且在不同治疗组间相似,实验期间未出现与CRS3123相关的严重不良事件。
目前来看,Crestone的CRS3123在针对CDI的治疗上,无论是有效性、复发率还是安全性上相较万古霉素等早期标准一线疗法已有不小的优势,未来可期。但同时,目前在万古霉素之上还有非达霉素这另一座大山,且全球CDI在研疗法众多。预计大概率Crestone的下一步将围绕其产品与非达霉素的竞争展开。
竞争格局:众多同适应症疗法中“突围”
很显然,目前的CDI治疗领域仍存在很大需求,已获批治疗药物一定程度上仍难以满足患者对降低复发率的需求。
而针对CDI在研疗法,全球范围内的研发思路主要分为两类,一者是沿用抗菌治疗的原有逻辑,只是将方向集中在了窄谱抗生素,比如非达霉素、CRS3123等;二者是针对CDI的免疫疗法,比如TCD单抗、CDI疫苗、粪菌移植(FMT)与干细胞等。
①窄谱抗生素
过去十年间,医学界对艰难梭菌感染(CDI)的病理生理机制,以及某些人群中高定植率等因素带来的诊断挑战有了更深入的认识。而如非达霉素等窄谱抗生素在临床应用上的普及,不仅能够有效控制急性感染,还能通过其独特的“窄谱”特性保护肠道微生态,减少对正常菌群的破坏,从而显著降低复发率,推动CDI治疗迎来显著改变。
目前,全球范围内用于CDI治疗的窄谱抗生素与抗菌药虽不少,但其中绝大多数临床后期(Ⅲ期)管线均难逃搁浅命运,比如Summit的Ridinilazole、爱可泰隆的Cadazolid、Cubist的Surotomycin等。
部分针对CDI的在研TCD单抗
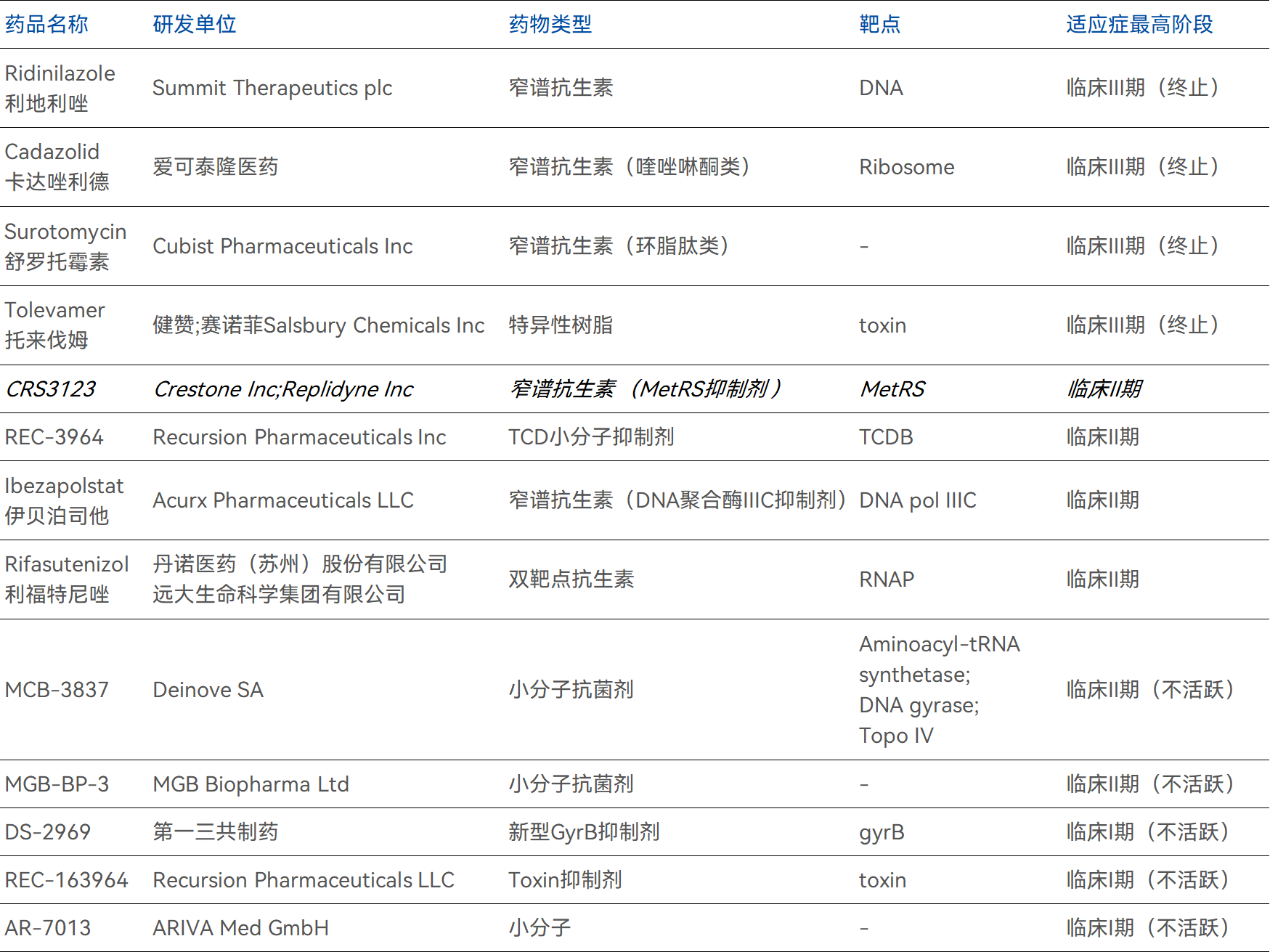
数据来源:药智数据
而在研活跃管线中,Crestone的CRS3123不仅是现阶段临床进展最快的管线之一,同时也是目前临床进展最活跃的管线之一,其未来极可能颠覆甚至重塑整个CDI的治疗格局。
② CDI免疫疗法
俗话说,解铃还须系铃人,既然艰难梭菌感染本质是人体肠道菌群微生态失衡,那么其解决办法除了采用新型抗生素灭菌外,恢复肠道菌群的动态平衡在一定程度也可达到治疗疾病的目的。
近年来,免疫治疗被视为应对CDI的新希望,该类型疗法强调增强宿主的免疫防御能力,直接对抗艰难梭菌毒素,或通过恢复肠道微生态平衡来减少感染的严重性和复发,代表疗法有粪菌移植恢复肠道菌群平衡、靶向细菌毒素的单克隆抗体、疫苗及干细胞治疗等。
粪菌移植
粪菌移植(Fecal Microbiota Transplantation, FMT)是一种通过将健康供体的肠道微生物群移植到CDI患者肠道中的方法,旨在通过恢复健康微生物群的多样性和数量,改善肠道屏障功能,其核心机制有二:
通过竞争性排斥作用占据肠道空间和营养来源,抑制艰难梭菌的过度生长。
通过健康微生物群的代谢产物调节免疫系统,这些代谢产物可作用于肠道免疫细胞,有效减少肠道的炎症反应。
临床研究表明,FMT对复发性CDI患者尤其有效,特别是在常规抗生素治疗无效时,它已被证明是一种安全且有效的治疗手段。
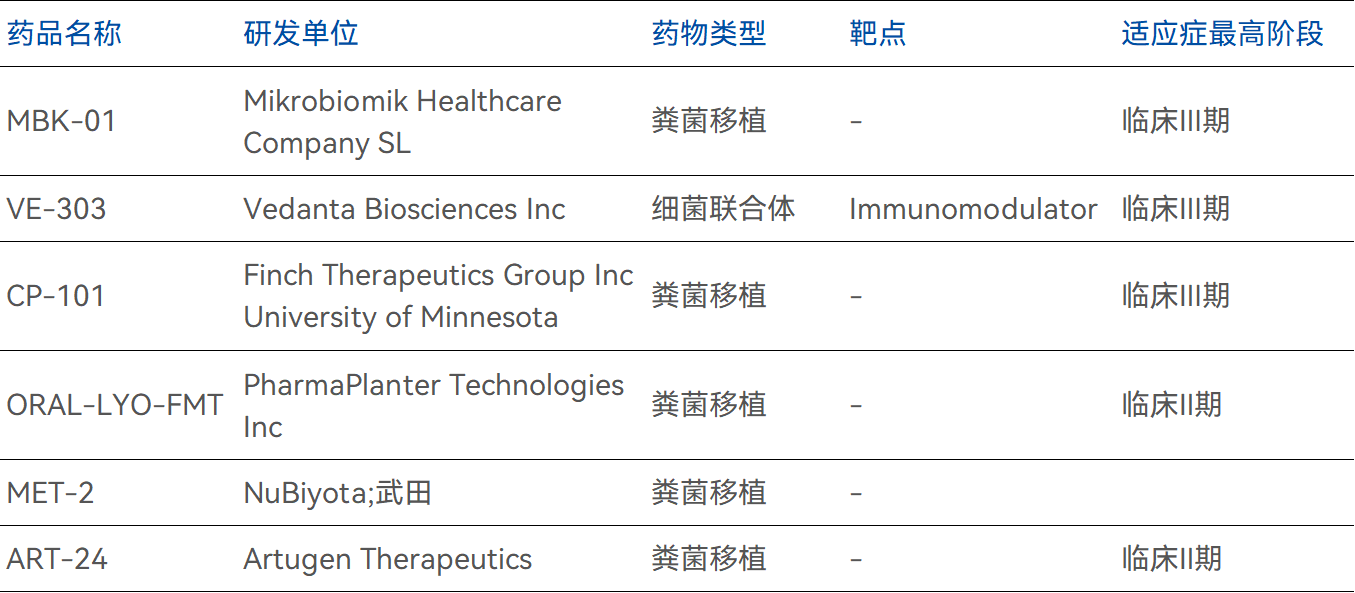
数据来源:药智数据
TCD单抗
该类疗法是一种专门设计来靶向C.difficile产生的毒素(Toxin A和Toxin B)的免疫疗法。其通过中和毒素,阻止其与肠道细胞的受体结合,从而减少肠道损伤和炎症反应。
目前,Medarex Inc的Bezlotoxumab是唯一获批用于治疗CDI的单克隆抗体,研究表明其可有效减轻CDI的复发,尤其是针对部分高风险人群(如老年人或免疫抑制患者)临床效益显著。
部分针对CDI的在研TCD单抗
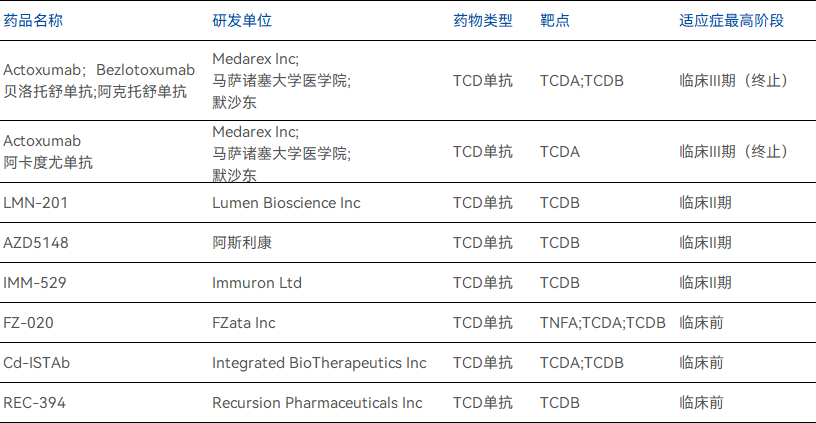
数据来源:药智数据
在研管线方面,目前全球范围内仅少数几款相关产品在研,其中Lumen BioscienceI的LMN-201、阿斯利康的AZD5148、Immuron的IMM-529临床进展相对较快,目前已处于临床II期,但以目前该类型疗法在指南中的地位来看,其短时间内或仍将处于辅助治疗阶段内。
而除了上述粪菌移植与TCD单抗外,CDI新药研发领域还有诸多如CDI疫苗、基因疗法、干细胞疗法等其他类型在研,疗法间作用机制也值得期待,比如CDI疫苗通过刺激宿主的免疫系统产生针对C.difficile毒素的保护性抗体,从而有效预防CDI的发生;而干细胞疗法则具备修复组织、再生肠道上皮细胞和免疫调节的能力。
但这一类疗法临床进展相对缓慢,管线多处于临床前期,短时间内很难对现有治疗格局产生影响。



