DDR赛道第二波:为何全球药企都在押注ATR?
在肿瘤治疗的靶向疗法浪潮中,DNA损伤应答(DDR)通路曾凭借PARP抑制剂的成功引领了黄金十年。从奥拉帕利获批上市至今,PARP抑制剂已在卵巢癌、乳腺癌等多个实体瘤领域确立了标准治疗地位,为携带BRCA突变的患者带来显著生存获益。但随着临床应用的深入,原发性耐药与获得性耐药问题逐渐凸显,约40%-60%的患者在治疗后会出现疾病进展,这成为制约PARP抑制剂临床价值的关键瓶颈。
因此,耐药困境下的行业开始将目光投向DDR通路更上游的核心调控分子——ATR(Ataxia Telangiectasia and Rad3-related,共济失调-毛细血管扩张和Rad3-相关激酶)。其作为复制应激应答的"总开关",在维持基因组稳定性中发挥不可替代的作用。
如今,从AZ到默克,从恒瑞医药到正大天晴,小分子ATR抑制剂正被视为“PARP之后的DDR新星”,已然成为全球研发布局的重点方向。
ATR的机制逻辑:
复制应激中的肿瘤脆弱点突破
DNA损伤应答(DNA Damage Response,DDR)作为细胞维持基因组稳定性的核心防御体系,主要包括碱基切除修复(BER)通路和同源重组(HR)/非同源末端连接(NHEJ)通路。而通常情况下,DNA修复的过程往往发生在损伤位点附近的染色质区域,其过程非常复杂,且伴随多种肿瘤发生,因此相关蛋白也是重要的潜在的药物靶点。
其中,PARP是单链断裂修复的关键分子,也是首个在临床验证的DDR靶点。其抑制剂通过阻断BER通路,使DNA单链损伤无法修复并转化为双链断裂,在HR缺陷(如BRCA突变)的肿瘤细胞中诱发“合成致死”,成功掀起了DDR靶向治疗的第一波浪潮。
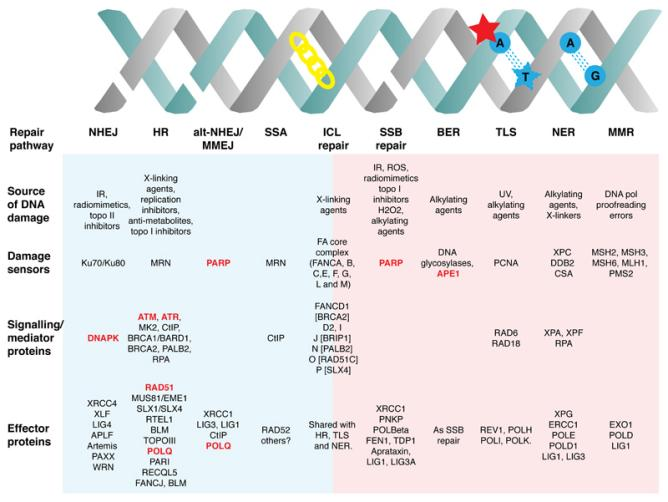
图1:DNA修复通路中主要传感器、信号传导和效应蛋白
图注:蓝色阴影区域表示双链断裂(DSB)修复通路;红色阴影区域表示单链断裂(SSB)修复通路,其中药物开发的主要靶点以红色标注[1]
而在复制应激及双链断裂修复环节中,ATR是DDR核心的关键激酶,负责感知复制应激(Replication Stress,RS)并将其信号传递至S和G2/M期检查点以启动DNA修复。ATR与DNA依赖性蛋白激酶催化亚基(DNA-PKcs),共济失调毛细血管扩张突变基因(ATM基因)构成了DDR的三大核心激酶。
而上述三者虽同属PIKK家族,其分工却有所不同:ATM与DNA-PKcs主要感应和修复双链断裂,而ATR则专责应对复制应激(Replication Stress, RS)——这是癌细胞在高速分裂、基因组不稳定背景下产生的核心脆弱点。ATR通过感知RS,启动CHK1等下游信号,参与DNA单链断裂修复,维持复制稳定性并防止细胞崩溃[2]。
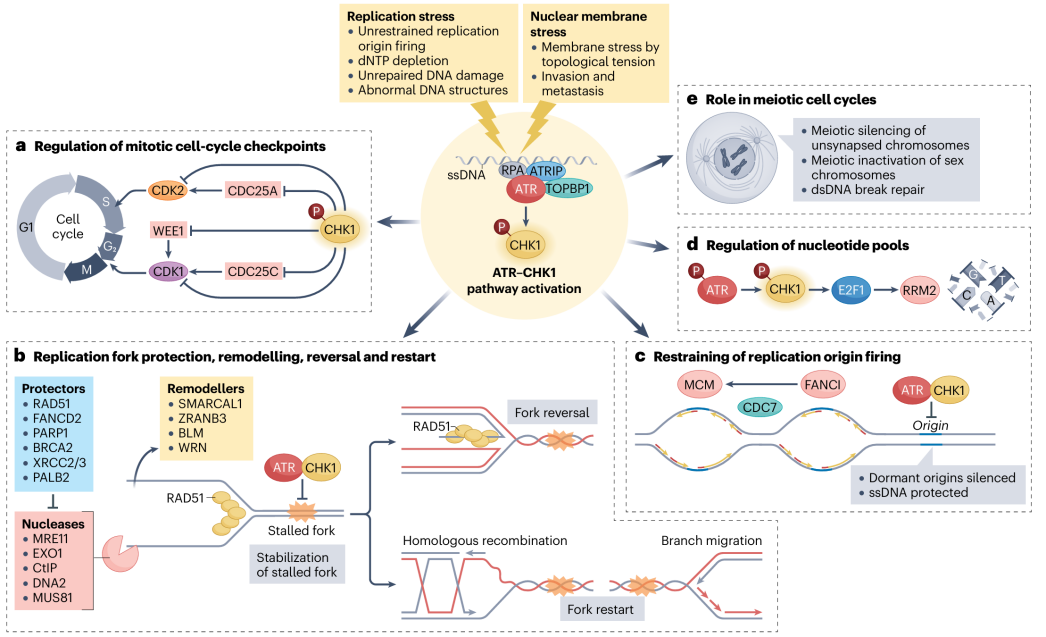
图2:ATR的生物学功能[2]
值得一提的是,ATM基因不是细胞存活必需的,人类ATM基因的突变会导致共济失调毛细血管扩张症的发生,其特点是小脑退化、免疫缺陷和癌症风险增加。但ATR是至关重要的,有研究表明ATR双等位基因的丧失会导致早期胚胎致死。
因此,ATR的选择性抑制为肿瘤治疗提供了新的思路,也为肿瘤研究提供了新的工具,目前,ATR抑制剂(ATRi)主要是通过两条途径进行临床应用开发。
第一条:
寻找预测性生物标志物来识别对单药治疗特别敏感的肿瘤
该途径是通过寻找预测性生物标志物(如ARID1A、ATM)来识别对单药治疗特别敏感的肿瘤。管线代表有:Berzosertib(M6620/VE822)、Ceralasertib(AZD6738)、Elimusertib(BAY1895344)、M1774和RP-3500(Camonsertib)。
其中,阿斯利康的Ceralasertib在Ⅱ期临床研究的初步结果表明,在ARID1A缺乏实体瘤患者中,Ceralasertib单药显示出具有良好的抗肿瘤活性(160mg,1日2次,口服d1~14,28d为1个周期),客观缓解率(ORR)为20%,观察到2例完全缓解(CR),这两例患者仍在接受治疗,持续缓解时间分别为19.8+个月和14.7+个月,且完全缓解状态仍在持续。另有1例患者因疾病稳定(SD)持续治疗8.8个月,Ceralasertib单药的总体临床获益率(缓解或疾病稳定持续>6个月)为30%[4]。
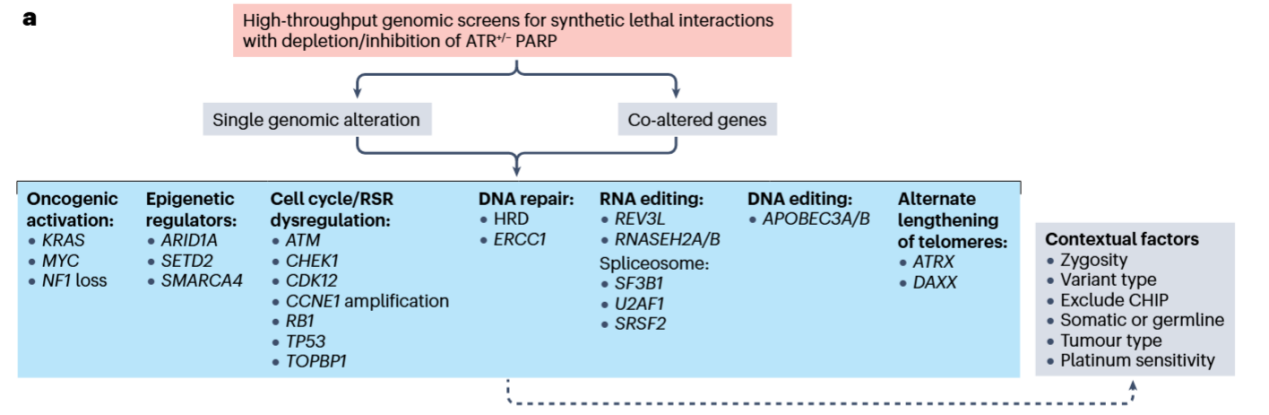
图3:ATR抑制剂敏感的潜在生物标志物[2]
第二条:
探索与其他药物联合用药的策略
① 与化疗联合
例如吉西他滨(Gemcitabine),吉西他滨联合Berzosertib组的中位无进展生存期为22.9周(90%CI 17.9-72.0),而吉西他滨单独使用组的中位无进展生存期为14.7周(9.7-36.7)(HR 0.57,0.33-0.98;单侧对数秩检验p=0.044;上单侧90%CI 0.87 [5];此外还有铂化合物[6-7]、拓扑替康类[8-9]等等。
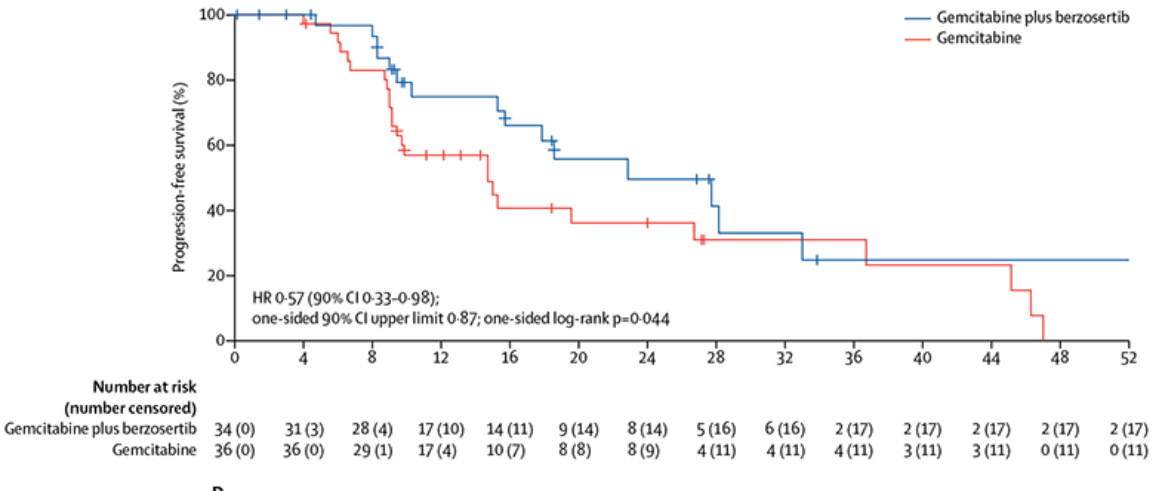
图4:吉西他滨联合Berzosertib治疗铂类耐药高级别浆液性卵巢癌[5]
② 与PARP抑制剂(PARPi)联合
一些临床前研究表明,PARPi与ATRi在卵巢癌患者中具有协同作用。这种协同作用存在于野生型和BRCA1、BRCA2突变的肿瘤中,但在野生型肿瘤中更明显。ATR抑制可能是克服PARPi耐药性的关键机制,包括恢复HRR缺乏、复制叉稳定、SLFN11失活和PARG表达缺失,其分子机制可能是pATR和pCHK1水平降低,RAD51募集减少,pH2AX积累增加。
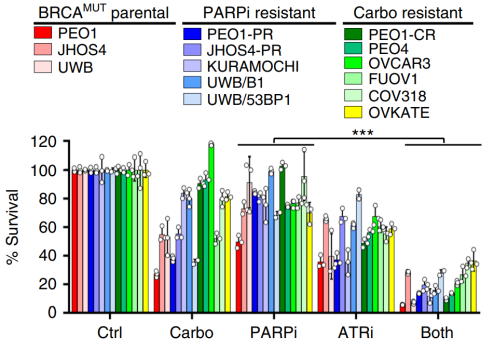
图5:PARPi–ATRi处理能显著降低肿瘤细胞活力[10]
同时,一项CAPRI试验评估了Ceralasertib联合Olaparib对铂类敏感并经过至少6个月的PARPi治疗后进展的卵巢癌患者的疗效,在13例患者中6例患者达到部分缓解,ORR为46%[11]。
③ 与免疫疗法联合
一项Ⅱ期试验评估了Ceralasertib联合Durvalumab治疗既往PD-1治疗失败的晚期/转移性黑色素瘤患者,结果显示ORR为30%,30例患者mPFS为7.1个月(95%CI,3.6-10.6个月);在数据截止时,30例患者中有14例死亡,中位OS为14.2个月(95%CI,9.3-19.1个月)[12]。
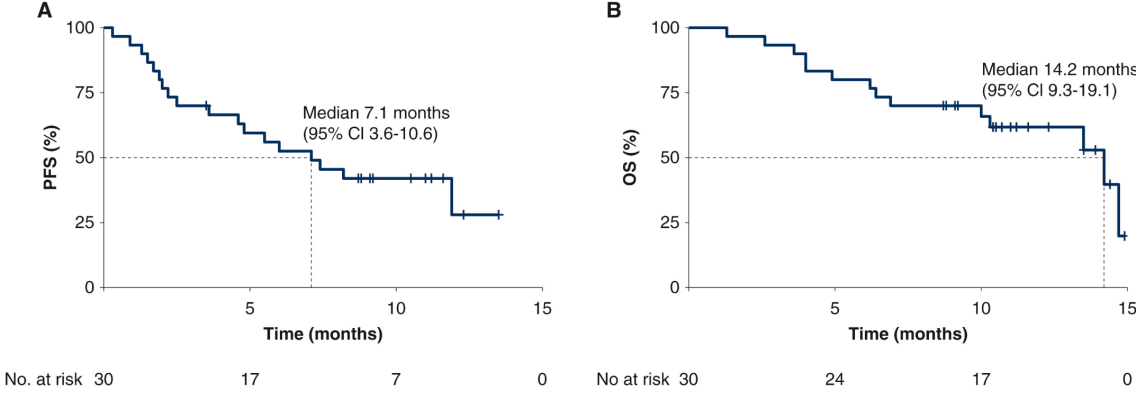
图6:Ceralasertib联合Durvalumab治疗黑色素瘤患者结果图[12]
综上所述,ATR抑制剂在肿瘤治疗上之所以能拥有如今地位,其两大核心亮点功不可没,一者是特异性杀伤,原则上仅在DNA修复缺陷(如ATM缺失)或高复制应激的肿瘤细胞中发挥毒性,对正常细胞损伤极小;二者是逆转肿瘤耐药性,研究数据证明,ATR抑制剂铂类化疗耐药和PARP抑制剂耐药的肿瘤拥有显著活性,尤其是KRAS+STK11/LKB1+KEAP1三突变,也可逆转免疫治疗耐药,重建抗肿瘤免疫。
目前,ATR已成为当前DDR靶点中最具系统性扩展潜力的方向之一,覆盖小细胞肺癌、三阴性乳腺癌、卵巢癌、胃癌/食管癌等多种常见肿瘤类型。
全球研发格局:
巨头领跑,20款候选药角逐临床
截至2025年,全球已有约20个ATR抑制剂进入临床阶段(表1,仅统计活跃管线,近三年有研发进展),其中以阿斯利康的Ceralasertib进展最快,目前已经进展至临床Ⅲ期,其次是默克的Berzosertib和Tuvusertib,目前均处于临床Ⅱ期。
表1 全球ATR靶点药物研发进展
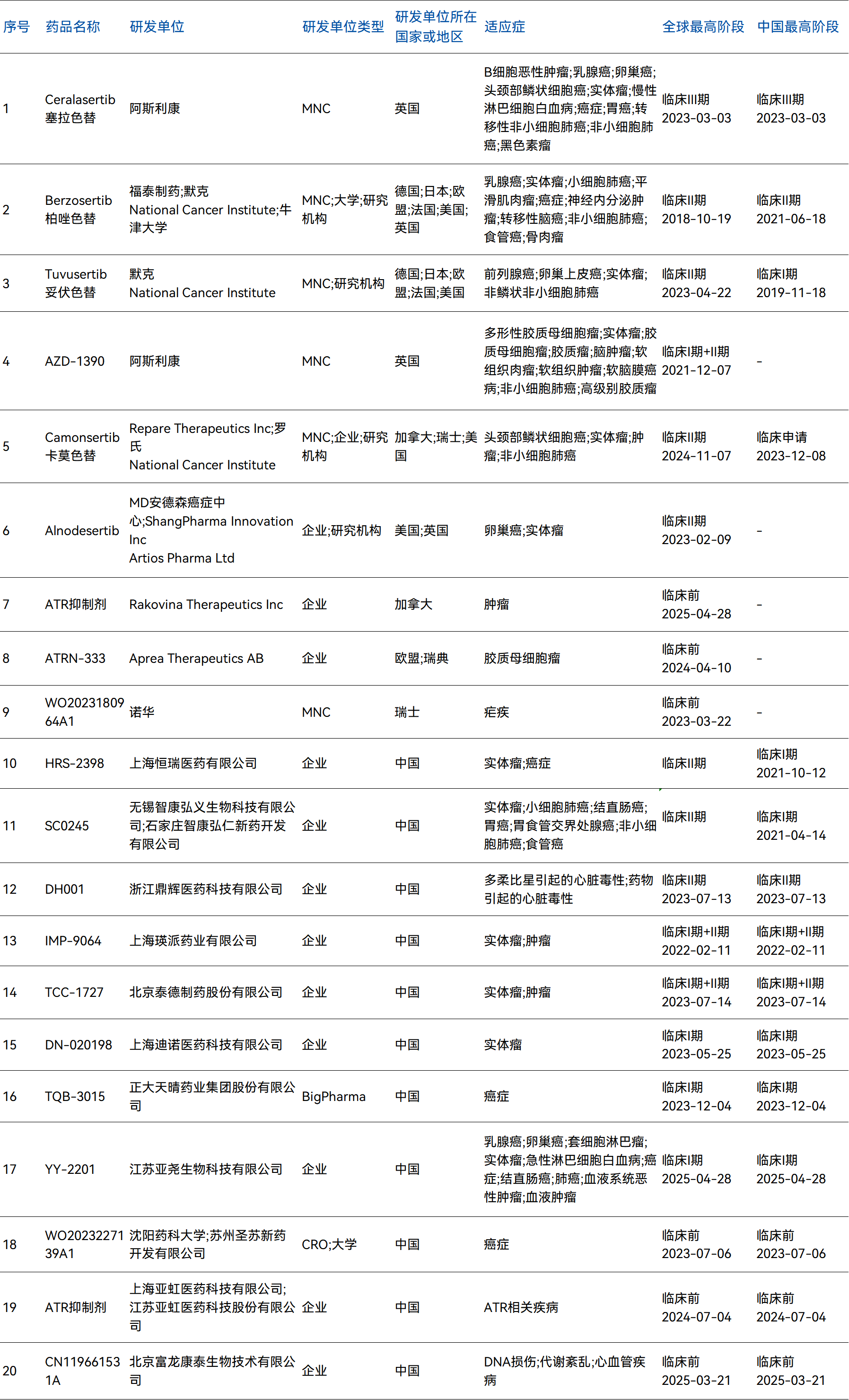
数据来源:药智全球药物研发系统(如有错误请指正)
具体来看,阿斯利康开发的高选择性ATR抑制剂,即Ceralasertib(AZD6738)研发重点聚焦于复制应激高(RS-high)或DNA修复缺陷(如ATM缺失、HRD)肿瘤,在与PD-L1抑制剂Durvalumab、PARP抑制剂及化疗/放疗联合时表现出良好的耐受性和初步疗效。
多项研究显示,ATM变异患者获益显著,验证了其“合成致死”作用机制。当前,Ceralasertib被视为继PARP抑制剂之后DDR领域最具潜力的下一代靶点药物,有望在精准分型和联合治疗策略中拓宽抗癌新路径。
表2 Ceralasertib临床试验汇总时间表
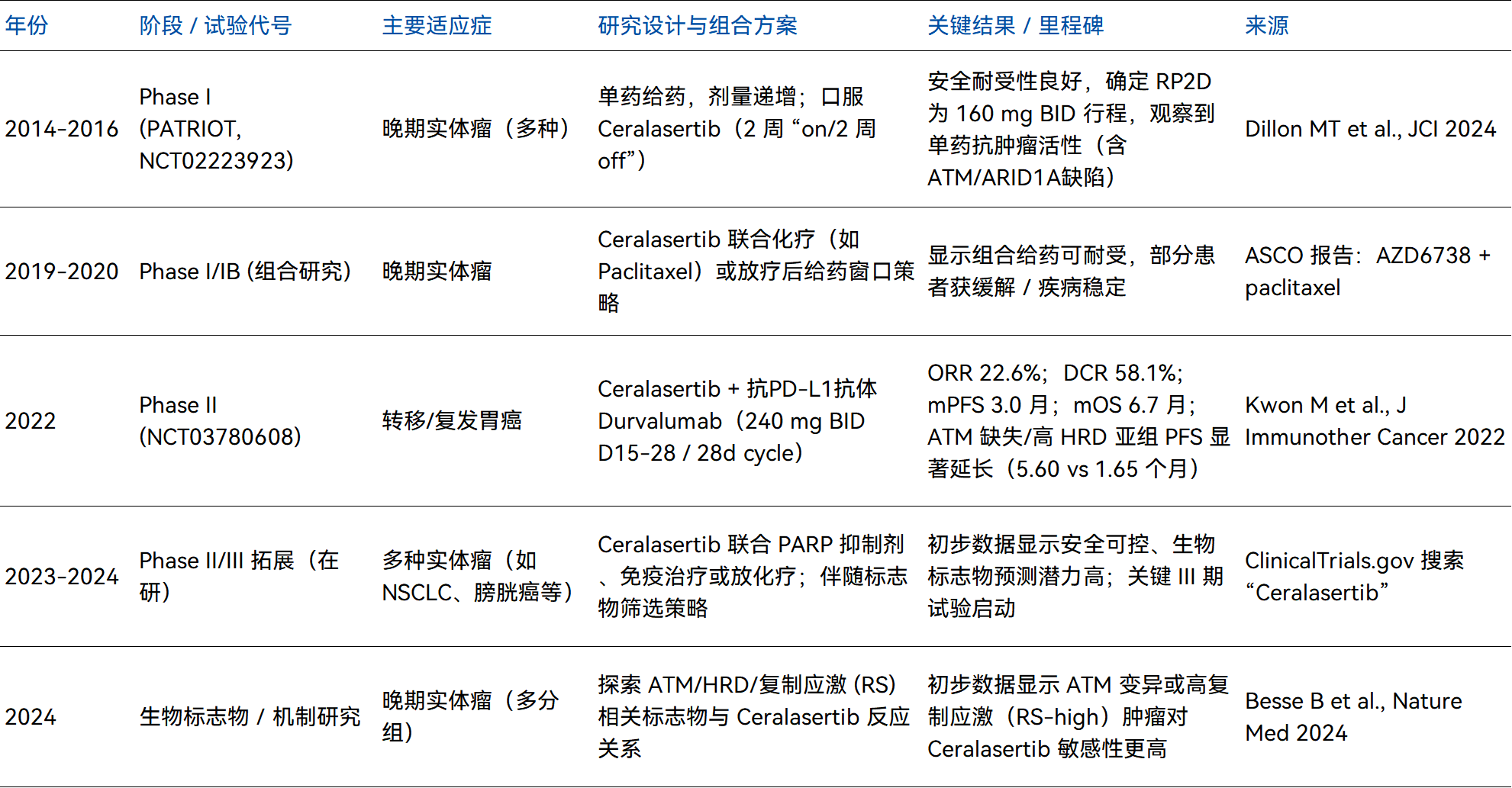
数据来源:公开资料整理(如有错误请指正)
默克Berzosertib(M6620)
Berzosertib早期联合化疗显示出较好的肿瘤缩小率,被认为是首批“可临床证明概念”的ATR抑制剂之一。
在单药治疗晚期实体瘤患者疗效的I期临床试验结果ORR为19%(4/21),所有4例患者均同时携带ATM的缺失或变异,但其中81.8%的患者出现ATRi的常见不良反应3级贫血,提示1例携带BRCA1致病突变,并对PARPi耐药的患者得到了长期缓解[13]。而关键临床Ⅱ期试验数据显示,在2023年1月27日的数据截止时(从初步分析开始>额外随访30个月),吉西他滨/贝佐塞替布组的中位OS为59.4周,而吉西他滨单用组为43.0周(HR 0.79,90%CI 0.52-1.2,单侧对数秩P=.18)。展现出吉西他滨/ATRi联合治疗铂类耐药卵巢癌的前景[14]。
表3 Berzosertib临床试验汇总时间表
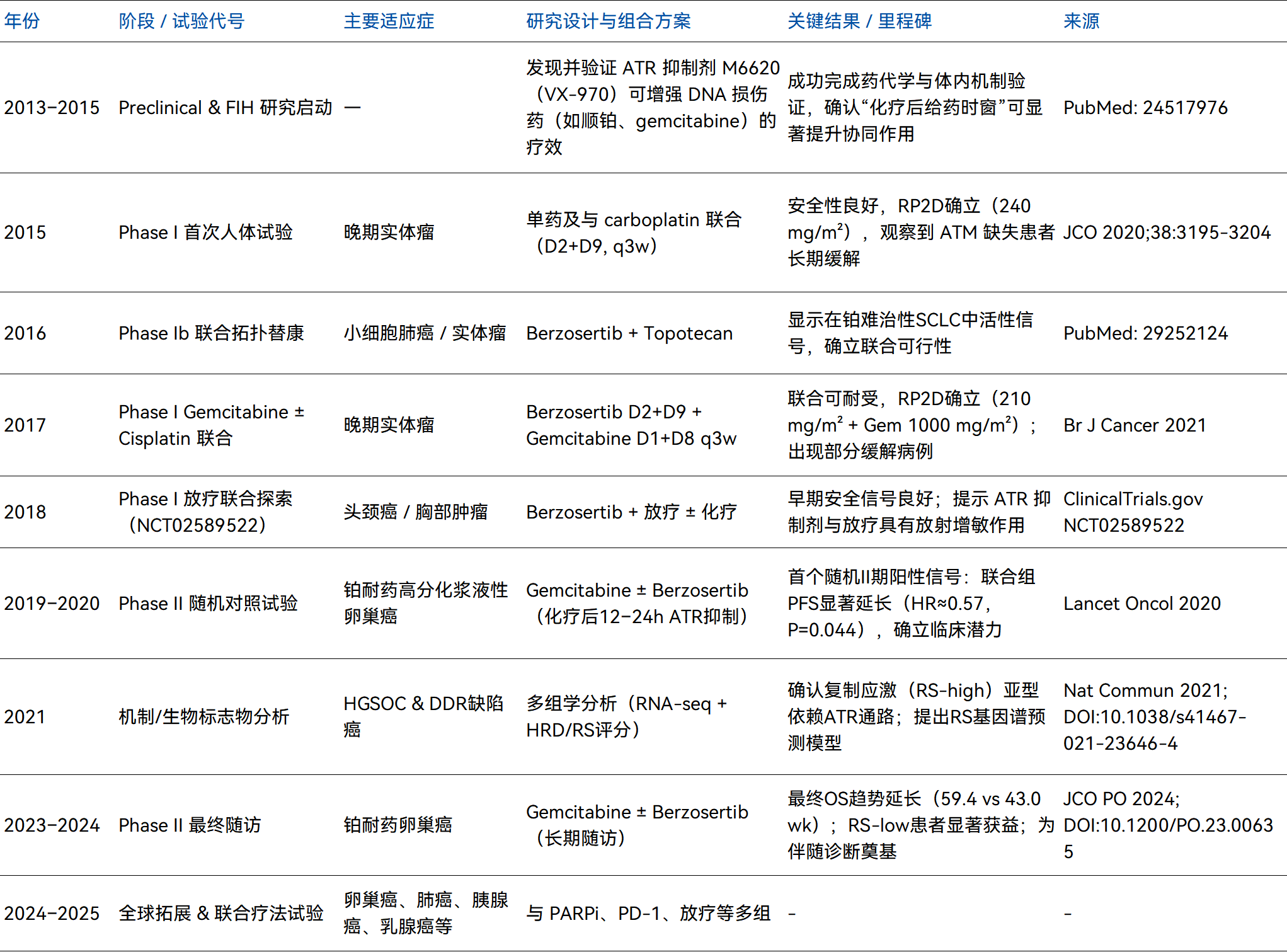
数据来源:公开资料整理(如有错误请指正)
两者对比来看,Ceralasertib是小分子口服ATR抑制剂,高选择性抑制ATR-CHK1通路以阻断复制应激修复,对ATM缺陷肿瘤、HRD阳性肿瘤选择性更强,更易与PD-1/PD-L1、PARP抑制剂联用,能有效突破PARP抑制剂耐药困境,且产业链完善、研发进展领先;而Berzosertib是靶向ATR的静脉注射小分子抑制剂,通过抑制ATR激酶活性诱导复制叉崩溃和细胞死亡,对复制应激显著升高的肿瘤敏感度更高,主要与吉西他滨、顺铂等化疗药物联用,虽早期开发领先,但后期推进稍慢。

数据来源:公开数据整理
其他产品例如罗氏的RP-3500(Camonsertib)在具有DDR基因变异的实体瘤患者中的Ⅰ/Ⅱ期临床试验结果显示在卵巢癌患者中ORR为25%(5/20),其中17例为铂类耐药,18例曾接受过PARPi治疗,也具备较高的潜力。
从整体研发趋势看,ATR正从“验证疗效”转向“优化耐受性+靶向精准化”的第二阶段。
中国进展:
从跟随到同步
近年来,国内药企在DDR领域的布局明显加快。
药智数据显示,已有超过7个ATR抑制剂项目在研,其中不乏领军企业:
恒瑞医药(HRS-2398):HRS2398缓释片是一款新型、高效、口服的ATR抑制剂,能够有效抑制ATR激酶活性,加剧DNA双链损伤,抑制细胞增殖,发挥抗肿瘤作用。2024年4月HRS2398国内获批临床,拟用于治疗晚期恶性肿瘤患者。目前全球最高阶段为临床Ⅱ期,中国最高阶段为临床Ⅰ期。

图片来源:CDE官网
中国生物制药(TCC1727):临床前研究显示,TCC1727单药表现出较好的安全性和疗效,与化疗药和PAPR抑制剂等药物联合时表现为协同抗增殖的作用。目前正在开展TCC1727联合贝莫苏拜单抗/奥拉帕利/托泊替康治疗晚期实体瘤的开放性、多中心Ⅰb/Ⅱ期临床试验。
正大天晴(TQB-3015):2023年11月已获CDE批准开展药物临床试验,拟用于治疗晚期恶性肿瘤,目前正在临床I期。
智康弘仁(SC0245):国内较早开始单臂、开放性、多中心的Ib/Ⅱ期临床试验的ATR抑制剂,SC0245口服片剂(ATRi)联合盐酸伊立替康注射液(TOP1i)治疗,研究病例多中心/Ib剂量递增约3-27例,Ib剂量扩展约10例,Ⅱ期30例正在开展中(CTR20223363)。
相较PARP的仿制潮,国内ATR方向目前仍处于原创窗口期,中国研发力量有机会跟上国际节奏,实现同频发展。



