WCLC上崭露头角的Biopharma
2024半年报数据显示,信达生物从营收上真正实现了第二增长曲线,从2022到2023年上半年同比不太显著的增长中彻底走了出来,实现了非常惊艳的商业化放量——2024H1营收达到了39.52亿元,同比增长46.3%。
而另一方面,这家行业内公认的“创新药二哥”,在2024世界肺癌大会(WCLC)上代表中国创新药发出中国声音,让世界为我国自主研发的first in class所震撼。
半年报漫谈
今年信达的半年报同比去年是一个很不错的对比,基本可以看出信达已经度过了精兵简政的瓶颈期,今年大规模的研发和销售投入既可以看成对未来预期乐观的表现,也是之后更大规模放量的前奏。

图片来源:信达生物2024上半年财报
从研发来看,今年上半年的研发费用从去年同期的9.23亿飙升到13.99亿,同比增长51.65%。这其实可以从更前期的研发费用窥见端倪:2021年和2022年信达生物的研发费用为10.42和11.74亿,也就是说,从2022年到2023年,信达生物的研发费用经历了一次较为显著的缩减。如今研发费用大规模地扩增,可以视为其作为biopharma对自身未来乐观预期的一大重要印证。
值得注意的是,信达生物的销售费用也在大规模递增。作为biopharma,它的经营核心之一就是几款单品的适应症扩增和商业化放量,因此销售费用的递增速度是其对未来商业化扩张速度的预期之一。站在今天的角度来看,信达的管理-销售费用在前面两年的上半年经历了平台期,都在13亿-14亿元之间,而今年的管理-销售费用开始了明显的再次增长:达到了今年H1的18.79亿元,同比去年H1上涨了39.48%。
当然,研发和销售大幅度增长的乐观预期是需要底气的,这个底气来源于2023年营收突破了前面两年的平台期,直接从45亿元左右突破了60亿元大关。这是个非常好的现象,营收增长让其可以更大规模投入研发和销售,在营收上继续贡献更可观的业绩,形成正向循环。
回溯完研发和销售费用后,再去总的看H1的营收业绩,会发现其营收爬坡还没有到平台期:今年的销售费用大幅度增长换来了今年上半年营收飙升至39.52亿,商业化投入取得了显著的成果。
此外,营收结构上,也较2023年发生了变化。2023年H1的营收中,产品销售收入为24.58亿元,今年同期为38.11亿元,同比增长了55.1%,也就是说,产品销售增长的幅度大过了营收增长的幅度,象征着信达作为biopharma而言营收结构的渐进式改善。此外,还有规模效应带来的生产成本上的优化:今年H1信达的毛利率为82.9%,相较去年同期上涨了1.6个百分点,这是很典型的生产规模放量带来的生产成本降低的体现。
即将商业化的潜在BIC
目前,信达有多项单品刚刚获批及正在进行上市审评,在今年下半年与明年上半年,将能看到数个商业化的新单品。
其中,氟泽雷塞已成为先锋。作为全球第三款KRAS G12C抑制剂,它已经用临床数据展现best in class的潜力。
今年8月21日,信达引进的差异化小分子药物氟泽雷塞(管线代号:IBI351)获批上市,是国内首个KRAS G12C抑制剂,用于二线及以上治疗晚期NSCLC患者。KRAS是RAS基因家族中的一类(RAS是第一个被人类发现的肿瘤基因),作为致癌基因来说,KARS基因突变是RAS基因突变中最常见的情况,占RAS基因突变总数的85%,在非小细胞肺癌中,30%的患者存在KRAS突变。
如果再细分到KRAS G12这个突变亚型的话,那么非小细胞肺癌中占比会进一步缩小些:KRAS G12C突变在美国的NSCLC患者中约占13%,在我国则约占4%。但是,作为基因突变而言,如果没有相关的小分子抑制剂开发,而仅仅是以化疗或IO疗法进行治疗的话,未免过于可惜。
而氟泽雷塞的出世,恰恰弥补了我国该领域的空白。该药的原研方是在KARS领域的深耕者劲方医药,氟泽雷塞是它的核心管线,倾注了多年的心血。2021年,信达生物以2200万美元首付款与开发支持费用+里程碑付款总计2.9亿美元从劲方医药手里引进,获得了氟泽雷塞在中国地区的开发和商业化权利,并在全球开发和商业化权益上拿到了一个可以选择的期权。
氟泽雷塞的获批主要基于其临床II期研究。该项II期临床的结果已发布于著名肿瘤期刊《Journal of Thoracic Oncology》(IF=21)上。根据II期临床的数据,116例患者入组,接受600mg剂量药物的治疗。临床结果上,确认的ORR达到了49.1%,DCR达到了90.5%,mPFS为9.7个月,12个月PFS率为37.9%
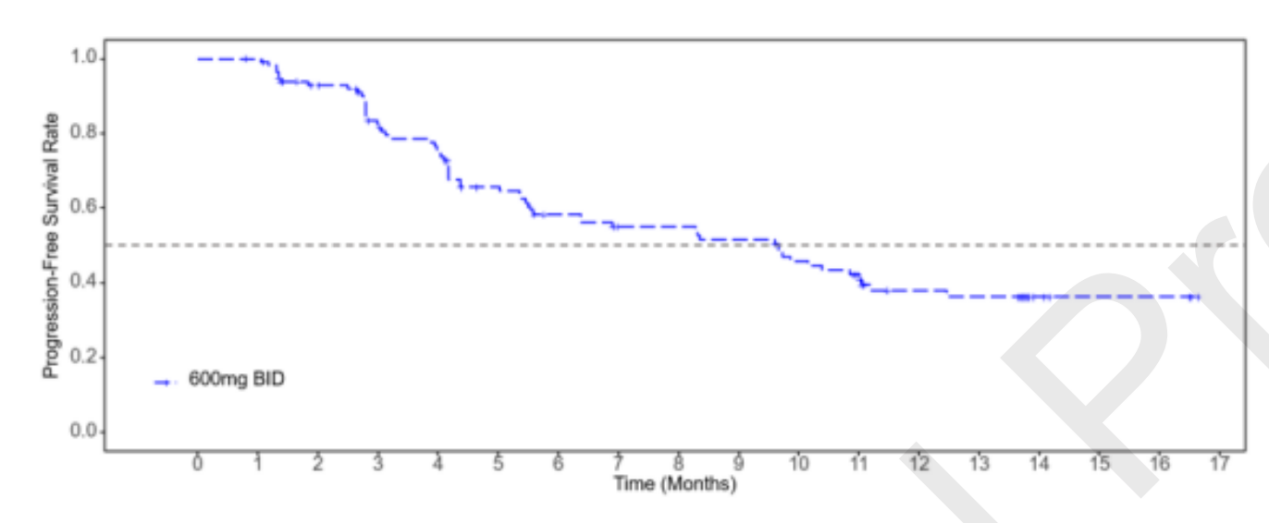
图片来源:《Efficacy and safety of KRAS G12C inhibitor IBI351 monotherapy in patients with advanced non-small cell lung cancer:results from a phase 2 pivotal study》
这比之前国外获批的两款KRAS G12C抑制剂疗效要优异很多,已上市的两款药物Sotorasib与Adagrasib二线治疗相关突变NSCLC的ORR约为40%,而mPFS约为五到六个月。
氟泽雷塞,正在展现它作为潜在best in class的潜力。
WCLC大会崭露头角
信达已经在今年的半年报中非常明确地阐述了其在肿瘤领域的发展战略:IO+ADC联用。IO疗法方面,用双靶点药物去迭代如今商业化的单靶点药物,去开发新一代的免疫疗法,ADC方面,去与全新的ADC平台合作,用更新一代的linker以及payload去武装下一代的ADC药物,例如在2021年与Synaffix开展技术平台的合作,专门用其新一代的糖基化偶联的技术来开发新一代的ADC,信达的CLDN18.2 ADC药物IBI-343便是出自此手笔。
近日,信达的一款双抗,再次让抗体研发圈炸了锅。IBI-363,这款靶向PD-1和IL-2(biaα)的双抗有着塑造未来以PD-1为基础的双抗疗法格局的潜力。这款充满变革类型的药物,已经在今年WCLC中崭露头角。
以PD-1为基础的双抗并不为奇,拉近视角来看,康方生物的PD-1/VEGF双抗AK112已经开始了商业化历程。但目前PD-1为基础的双抗仍然处在探索阶段,未来癌种适应症能覆盖多广,能不能像K药一样“万癌皆可用”,能不能达到优于单抗治疗的目的,还是研发界正在探索的热点。
而IBI-363的作用机制与AK112并不相同,它主要的方向并不是在于免疫检查点抑制和抗血管生成之间的协同作用,而是用IL-2这一靶点去更大程度促进T细胞活化和增殖。要知道,IL-2此前的名字是T细胞生长因子,它1976年被发现就是因为对T细胞的持续活化和延长其生存。
在此前,IL-2类型的药物一直要面临毒性强和半衰期短及激活Treg细胞的问题,Treg细胞的(调节型T细胞)主要作用是抑制体内杀伤性T细胞的增殖,而激活Treg细胞主要靠的就是α受体(CD25),以之前的研发思路,都是尽可能避免IL-2单抗和α受体的结合,以避免其激活Treg抑制免疫反应。
而信达的思路则非常有意思:反其道而行之,专门结合让该双抗结合α受体。这里面的奥秘在于肿瘤特异性CD8+T细胞同样具有CD25受体,对IL-2单抗会敏感,而根据信达发在《nature cancer》上的文献,其已经对IL-2 biasα方面的机制有了比较系统的阐述。
最重要的一点:IL-2R biasα激动剂可提高肿瘤中效应T细胞与Treg细胞的比率,这是个非常重要的发现,表明其对于肿瘤环境而言,首要作用是增强效应T细胞杀伤肿瘤的活性,而不是首要激活Treg细胞来抑制免疫力。
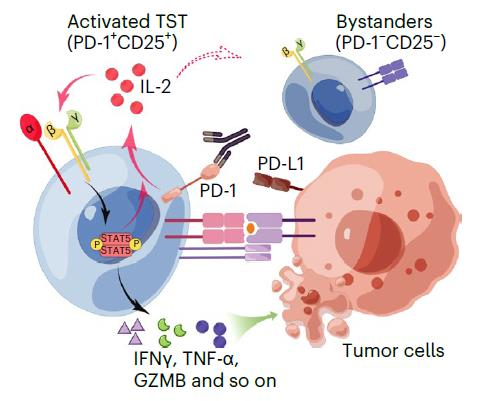
图片来源:IL-2Rα-biased agonist enhances antitumor immunity by invigorating tumor-infiltrating CD25+CD8+T cells
有了这个理论性突破为基础,剩下的延长半衰期等问题对于信达而言都不是难事。
目前,信达对该药的布局非常之广,其不仅期待于IBI-363用于大瘤种,更会将其主要用于“冷肿瘤”的突破上。
在WCLC上,IBI-363做了关于其在NSCLC适应症上I期临床结果的口头汇报。根据摘要,其一期临床纳入的患者就达到了89例。在鳞状非小细胞肺癌患者中(n=37,之前36位接受过IO疗法治疗,EGFR1例突变),ORR和DCR分别达到了35.1%和75.7%,mPFS达到了5.5个月。
而在高剂量组3mg/kg Q3W队列中,7例可评估疗效的患者中有6例达到部分缓解ORR高达85.7%。
当然,NSCLC只是它适应症中比较大的一部分,远不是全部,IBI-363的未来,是真正的星辰大海。
参考来源:
1.信达生物半年报
2.Efficacy and safety of KRAS G12C inhibitor IBI351 monotherapy in patients with advanced non-small cell lung cancer:results from a phase 2 pivotal study
3.IL-2Rα-biased agonist enhances antitumor immunity by invigorating tumor-infiltrating CD25+CD8+T cells
4.WCLC官网摘要:摘要号MA11.04



